1996年,世界上第一只克隆哺乳动物——多利羊的诞生,曾让世界为之震动,仿佛打开了一扇通往基因复制与生命“备份”新纪元的大门。然而,此后近三十年,克隆技术并未如预想般广泛进入农业或医疗应用,逐渐淡出了公众视野,给人一种“昙花一现”的印象。它真的失败了吗?还是说,其最深层的科学价值,才刚刚被揭示?
2026年3月24日一项发表于《自然通讯》的里程碑式研究《Limitations of serial cloning in mammals》为我们理解克隆技术的极限与生命繁衍的本质提供了前所未有的洞见。日本山梨大学的研究团队进行了一项长达近20年的实验,他们从小鼠身上提取体细胞,如同“接力赛”一般,用克隆出的个体再次提供体细胞进行下一轮克隆,试图回答一个根本性问题:哺乳动物能否仅依靠克隆(无性繁殖)来维持整个物种?

一场持续了58代的“克隆马拉松”
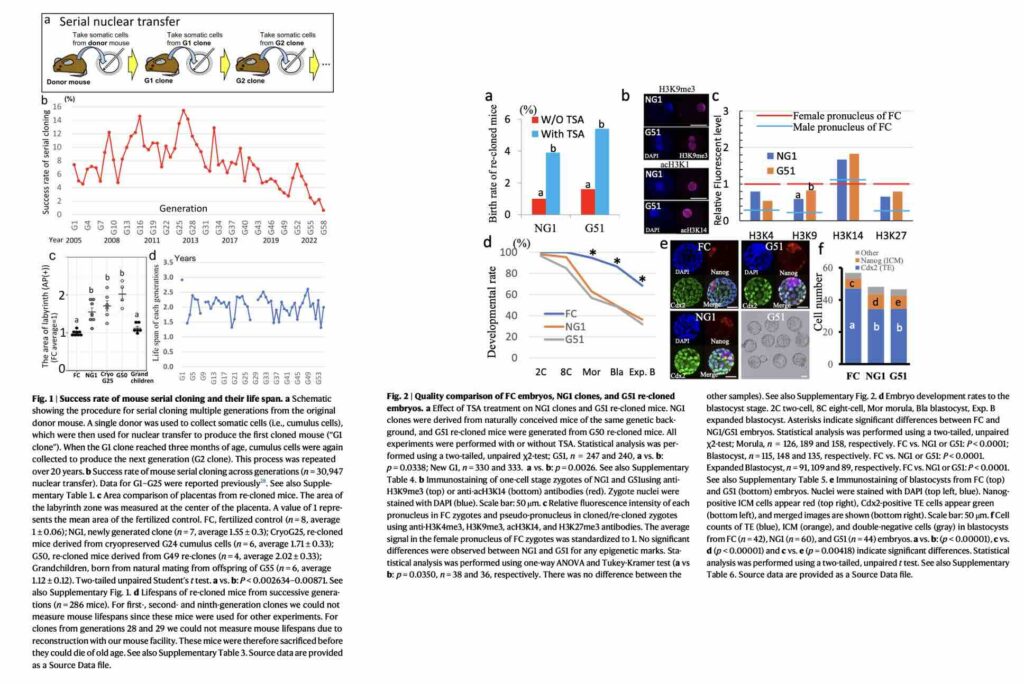
实验始于2005年,研究人员从一个供体小鼠开始,使用体细胞核移植技术,成功克隆出第一代(G1)小鼠。当这只克隆鼠成年后,他们取其体细胞,克隆出第二代(G2),如此循环往复,持续了20年。这项研究的规模空前浩大,总共进行了超过3万次核移植操作。
最初的成果令人鼓舞。在克隆到第26代时,成功率甚至还略有上升。克隆小鼠看上去完全正常,寿命也与普通小鼠无异。起初,团队甚至乐观地认为,连续克隆可以无限期持续下去。然而,随着实验进行到中后期,转折点出现了。克隆成功率从大约第27代开始下降,最终,克隆进行到第58代时宣告终结——所有第58代的克隆小鼠都在出生次日死亡。这表明,即便在实验室的完美条件下,克隆技术也存在其无法突破的内在极限。
隐形的代价:DNA中的“突变累积炸弹”
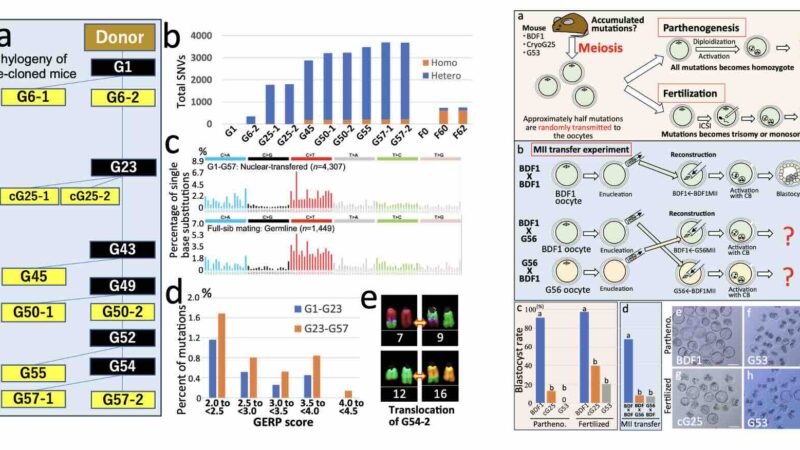
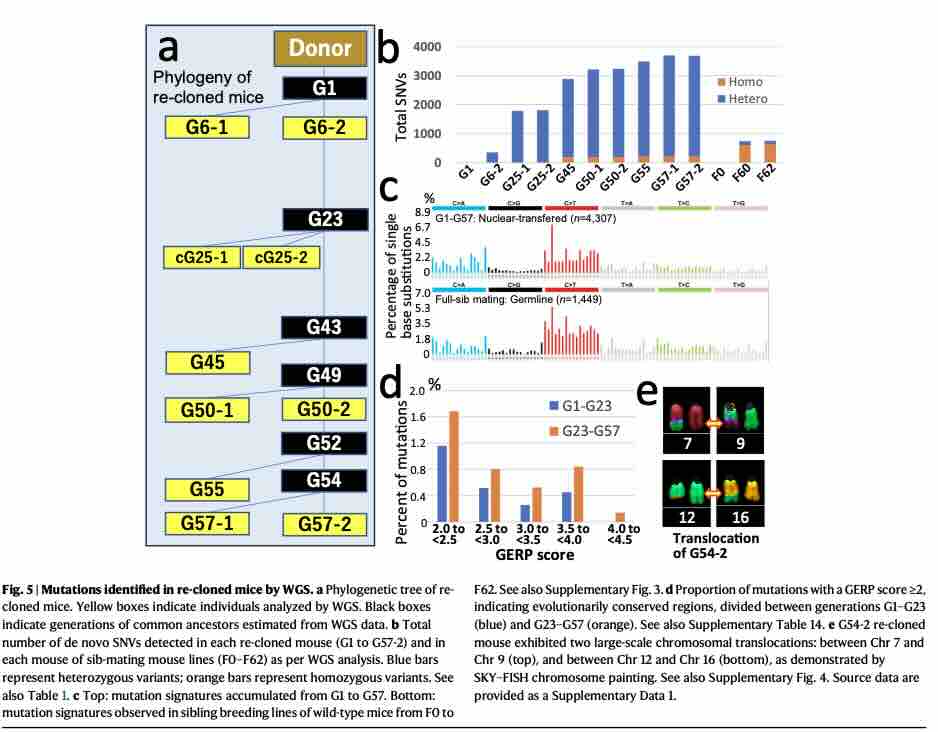
为了探寻克隆成功率最终崩溃的原因,研究者们对历代克隆小鼠的基因组进行了深度测序。结果揭示了一个令人不安的事实:尽管克隆个体外表健康,但每一次克隆过程都会在DNA中引入新的突变。
这些突变既有单核苷酸变异(SNVs),也有更大规模的结构变异(SVs)。平均而言,每传一代,基因组就会积累约70个SNVs和1.4个结构变异。随着代数增加,大量结构变异开始出现,例如大片段的染色体缺失、杂合性丢失,甚至一条X染色体的完全丢失。在第54代克隆鼠中,甚至观察到了染色体之间的易位(如7号与9号染色体交换片段)。
尤为关键的是,从大约第25代开始,这些突变中有害变异的比例显著增加。研究者将这些有害突变比作“莫勒氏齿轮”——这是一个经典的进化生物学理论,指在无性繁殖的种群中,有害突变会像齿轮只能单向转动一样,不断积累且无法被有效清除,最终导致种群“崩溃”。
性的救赎:为何性繁殖无法被替代?
既然克隆体自身似乎健康,那么问题出在哪里?后续实验给出了关键答案:问题出在生殖系统上。
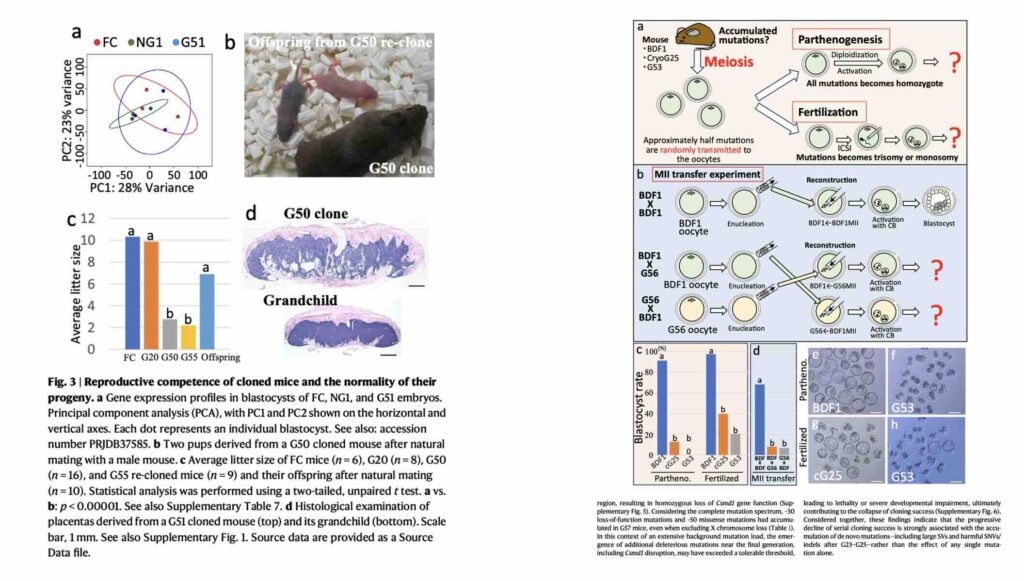
研究人员尝试让接近最终代(如G55代)的克隆鼠与正常雄鼠进行自然交配。尽管它们能产生卵子并受精,但产下的幼崽数量急剧减少,这意味着胚胎发育到后期大量死亡。然而,当这些(有缺陷的)克隆鼠生下的少数后代再通过正常的性繁殖生育孙代时,产崽数又恢复了正常。
这说明,克隆过程积累的“遗传债务”严重影响了克隆体生殖细胞(卵子)的质量,导致胚胎无法正常发育。但关键的性繁殖过程——减数分裂和两性基因组的结合——能够奇迹般地“筛查”并修复这些遗传异常,产生健康的下一代。
通过替换卵子的细胞核或细胞质的实验进一步证明,晚期克隆体的卵子无论在遗传物质(细胞核)还是细胞环境(细胞质)上都存在缺陷。
结论与展望:克隆技术并未退场,而是找到了真正的角色
这项历时20年的研究,首度在哺乳动物身上以令人信服的实验数据验证了“莫勒氏齿轮”假说,从遗传学层面解释了为何有性生殖是高等动物不可替代的繁衍方式——它是生命用来清除有害突变、维持基因组健康的必需机制。
因此,克隆技术的“销声匿迹”,并非技术本身的失败,而是我们对其能力和界限的认识变得更加清晰和深刻。它可能无法用于创造一个无需性别的物种,但其独特的价值正得以重新定义:
- 珍稀与濒危物种保护:克隆技术可以作为“基因急救箱”,从逝去或濒危个体身上恢复遗传信息,为种群注入宝贵的遗传多样性,但这之后,必须回归到自然的有性繁殖来维持种群的健康。
- 优质畜牧个体的快速扩繁:克隆可用于复制顶级种畜的优良基因,但扩大的群体依然需要通过常规育种来延续。
- 基础研究的利器:它依然是研究发育生物学、表观遗传重编程和衰老等生命核心过程的强大工具。本研究本身就是其价值的最高体现。
多利羊开启了克隆时代,而这项持续20年的克隆马拉松则为我们画出了一条清晰的技术与生命规律边界线。克隆技术没有退出历史舞台,它已从一个充满科幻色彩的“复制”工具,蜕变为一个帮助我们理解生命延续之奥秘、并在特定领域守护生物多样性的精密科学手段。它告诉我们,生命的延续,终究依赖于那场精妙而富有创造性的两性基因之舞。


